iPS細胞は、皮膚や血液といった細胞に特定の遺伝子などを働かせて作る。受精卵のように体のさまざまな細胞や組織に成長でき、ほぼ無限に増殖する。この特徴を生かし、病気や事故で失われた臓器の機能を取り戻す再生医療に使う研究が進んでいる。
ニュースな科学
京大の血小板輸血計画承認
iPS心臓・脳にも臨床
がん化・拒絶反応抑え加速
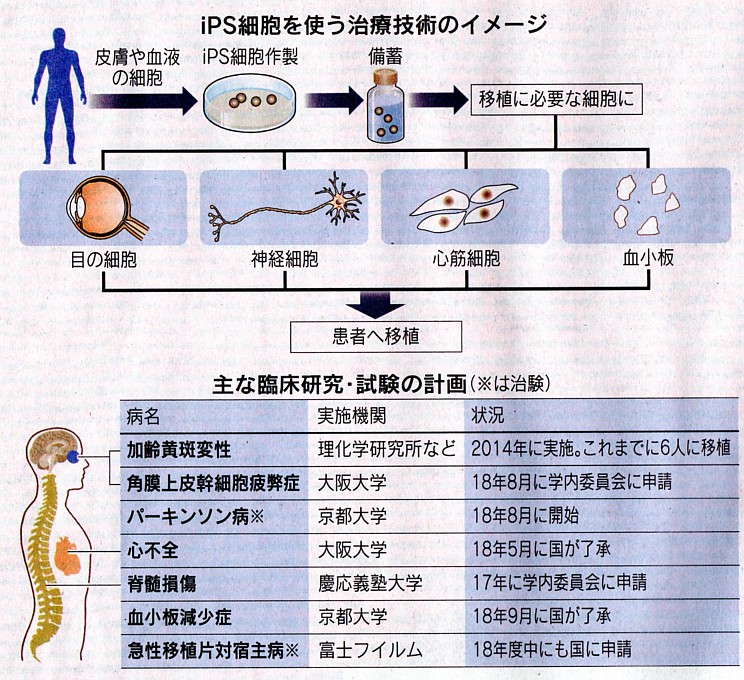
iPS細胞を実際の患者に使う臨床応用が広がっている。京都大学が血液成分の血小板を難病患者に輸血する臨床研究計画が21日、厚生労働者の専門部会で了承された。目、心臓、脳でも進む。富士フイルムなども2018年度中にも臨床試験(治験)を申請する予定で、企業での取り組みも活発になってきた。日本で生まれたiPS細胞による治療が、実用化へさらに一歩踏み出し始めた。

iPS細胞は、皮膚や血液といった細胞に特定の遺伝子などを働かせて作る。受精卵のように体のさまざまな細胞や組織に成長でき、ほぼ無限に増殖する。この特徴を生かし、病気や事故で失われた臓器の機能を取り戻す再生医療に使う研究が進んでいる。
他人の細胞を移植
臨床応用への先駆けとなったのが、理化学研究所などのチームの取り組みだ。2014年、iPS細胞から網膜の細胞を作り、目の難病「加齢黄斑変性」の患者に移植した。人に移植したのは世界初で、研究段階の治療法を試す「臨床研究」として実施した。
1例目は患者自身の細胞を使い、2例目からはあらかじめ備蓄しておいた他人のiPS細胞にした。患者一人ひとりに合わせるやり方は、培養や品質検査に膨大な費用と時間が必要だからだ。
iPS細胞は人為的に遺伝子を入れるため、がんになるリスクを抱える。移植用の細胞になり遁なった不完全な細胞が混ざると、がんになりやすい。最初に目の難病が選ぼれたのは、外から観察して異変を見つけられ、取り除く手術も難しくな小からだ。
これまでに他人のiPS細胞を使った移植で、患者1人が網膜が腫れる合併症を起こして手術を受けた。この事例も含めて、安全上の深刻な問題は起きていない。移植した細胞を患者の免疫が異物とみなす拒絶反応の問題も、拒絶反応を起こしにくい特殊な免疫型を持つ人のiPS細胞を使うことで抑えた。この成功をきっかけに、他の臓器への応用が進んだ。
この春以降、臨床応用を目指す計画が相次いだ。5月、大阪大学のチームが計画するiPS細胞から作った心筋シートで重い心不全の患者を治療する臨床研究を国が了承した。9月に国が了承した京大チームの臨床研究計画は、出血を止める血小板をうまく作れない「血小板減少症」の患者が対象だ。
保険適用を見据えた治験でも取り組みが始まった。京大病院が8月、徐々に身体が動かなくなるパーキンソン病の患者で開始。運動の指令を伝えるドーパミンと呼ぶ物質を出す神経の細胞をiPS細胞から作り、患者の脳に移植する。富士フイルムも18年度中にも、白血病の骨髄移植で起こる重い合併症「急性移植片対宿主病」の患者を対象とした治験を国に申請する。
真価は未知数
これまでの臨床応用の動きはいずれも、実績のある研究だ。iPSではない別の細胞を使う形で治療を試み、成果を挙げてきた。例えば、心臓は患者自身の太ももの筋肉細胞から作製して心不全の患者に移植しており、パーキンソン病は海外で堕胎した胎児の神経細胞を使った研究例がある。
一方、加齢黄斑変性の臨床研究と違い、多くの計画でiPS細胞の免疫タイプを患者と合わせて拒絶反応を低減する戦略は採らない。免疫抑制剤で拒絶反応を抑える。
特殊な免疫タイプのiPS細胞を使っても、心臓は拒絶反応が起きてしまう。神経は拒絶反応が弱いとされる。免疫抑制剤を使うと、移植したiPS細胞が生き残りやすくなり、治療効果が高まるという理由も大きい。患者自身の細胞を使う血小板では拒絶反応が起こらず、細胸に核がないためがんにならないという安全面での利点もある。
まだ、少数の患者で安全性を確認する段階だが、少しずつ治療効果の検証に移っていくだろう。目の角膜や脊髄損傷は移植によって、機能を失った組織や臓器が再生する効果が高いとみられている。ただ、少ない患者ではうまくいっても、多くなると効果がみられなくなったり、副作用が問題になったりすることもあり、真価は未知数だ。京都大学教授の山中伸弥さんは「一般的な医療になるまで10〜20年かかる」とみる。
キーワード
臨床研究と臨床試験
動物実験の結果などを踏まえて、人を対象に実施する医学的な研究が「臨床研究」だ。
目的は病気の予防や診断、新たな治療法、病気のメカニズムの解明など幅広い。iPS細胞のような高度な先端医療については、国のチェックを経て実施する。
中でも、新しい薬や医療機器の候補などを使う治療法の有効性や安全性を調べる研究は「臨床試験」と呼ぶ。このうち、企業が製品として製造・販売できるよう国に承認してもらうため、データを集める臨床試験が「治験」だ。企業が実施する治験は医薬品医療機器法(薬機法)に基づいて実施される。医師が主体的に企画・実施する形式のものは「医師主導治験」と呼んで区別している。
かがくアゴラ
大阪大学教授 紀ノ岡正博氏
再生医療、産業化へ広く連携
損なわれた臓器や組織の機能を修復する最先端の再生医療は、実用化に向け臨床研究などが進んでいる。技術を産業とするためには医療研究者や医師だけでなく、細胞培養や装置開発など様々な分野の人の連携が欠かせない。大阪大学の紀ノ岡正博教授はものづくり、人づくり、ルールづくりを合わせた「コトづくり」と呼ぷ社会システムの構築が重要だと話す。
政府は再生医療に力を入れており、2014年には薬事法を改正した医薬品医療機器等法と再生医療等安全性確保法が施行された。安全な再生医療や製品を円滑かつ素早く実用化するのが目的だ。経済産業省は国内の再生医療の市場規模が30年に1兆円になると試算している。
山中伸弥京都大学教授が開発したiPS細胞を使った目や心臓、脳の病気の臨床研究や臨床試験(治験)も始まった。ただ優れた素材や独自技術があってもそれだけでは普及は難しい。
私の専門とする化学工学は範囲は広く、素材をもとにどうやって製品を世の中に出すかを考える分野だ。再生医療を支え、産業化のための流れをつくり出す、その調整をする番頭役が仕事だと思っている。
もともと不安定な細胞を使い品質が高く安全な再生医療製品をつくることはものづくりの一つだ。細胞を無菌状態で自動培養するシステムを開発している。各工程を分け、機器同士を最適に接続することで製造コストを現在の10分の1にできる。
大阪大学は企業から人を集めて再生医療を理解した製造工程の設計ができる人材を育成するための講座も開いている。私が理事を務める日本再生医療学会では細胞培養に携わる臨床培養土の認定制度も14年に始めた。
産業化にはルールづくりも欠かせない。日本人はルールがない場で新たな製品を生み出すのが苦手だ。細胞培養などでまずルールをつくり、国際標準化を目指すことが重要だ。日本の立ち位置の確保にもつながる。